Изучение и сравнительная оценка гидрохимических и биохимических способов переработки сырья, содержащих уран, золото и сопутствующие цветные металлы
Гидрометаллургические технологии сейчас достаточно широко используются в промышленном масштабе для переработки сульфидных руд и концентратов, содержащих цветные и благородные металлы. В настоящее время внедрение таких процессов в производство особенно актуально из-за ряда проблем, с которыми сталкивается горная и металлургическая промышленность, включая истощение запасов богатых и легкообогатимых руд, что заставляет активно вовлекать в переработку упорные, бедные, забалансовые и труднообогатимые руды, упорные и некондиционные концентраты и отходы обогащения и металлургического производства. Технологии, основанные на процессах биовыщелачивания (биогидрометаллургические технологии), внедрены на предприятиях, расположенных по всему миру, и вносят значительный вклад в добычу многих металлов.
Ранее исследовательской группой настоящего проекта были достаточно детально изучены вопросы извлечения благородных и цветных металлов, включая золото, с использованием процессов биокисления, биовыщелачивания и двустадийного кислотного выщелачивания, позволяющих повысить степень извлечения как цветных металлов, так и золота. Данные вопросы также остаются актуальными в рамках проводимых исследований рабочей и в настоящее время. Исследователи рабочей группы также продолжают работать в данном направлении, в связи с его высокой практической значимостью.
Основой процессов биовыщелачивания сульфидных руд являются процессы биоокисления железа и серы, которые являются компонентами сульфидных минералов микроорганизмами различных таксономических групп. Общими свойствами микроорганизмов, которые осуществляют процессы биовыщелачивания сульфидных минералов, является способность окислять серу и железо для получения энергии для жизнедеятельности, ацидофилия (оптимум для их активности лежит в диапазоне pH ниже 3) и устойчивость к высоким концентрациям ионов металлов и металлоидов в среде. Несмотря на наличие общих физиологических свойств микроорганизмы, осуществляющих биовыщелачивания включают виды, различающиеся по оптимумам температур, спектру окисляемых субстратов, а также по используемым источникам углерода для конструктивного метаболизма (диоксид углерода и органические вещества). Широкий диапазон условий, в котором активны микроорганизмы, окисляющие сульфидные минералы, позволяет осуществлять технологические процессы с различными технологическими параметрами.
В основе биогидрометаллургических процессов лежит биоокисление сульфидных минералов, однако из-за особенностей минерального сырья различных металлов, биоокисление играет разную роль в их извлечение из руд и концентратов. Сульфидные руды цветных металлов (меди, никеля, цинка, кобальта) содержат минералы, непосредственно включающие в кристаллическую решетку ионы металлов (например, халькозин (Cu2S), ковеллин (CuS), халькопирит (CuFeS2), сфалерит (ZnS), пентландит ((Ni, Fe)9S8)). Их биоокисление приводит к переходу ионов цветных металлов в жидкую фазу: MeS + 2O2 биоокисление Me2+ + SO42−
Металлы из жидкой фазы могут быть извлечены различным образом (жидкостная экстракция, цементация, осаждение сульфидом) для дальнейшего получения товарной продукции.
В случае переработки упорных золотосодержащих руд и концентратов биогидрометаллургические процессы применяются для вскрытия тонковкрапленного золота, которое не может быть с высокой эффективностью извлечено с помощью прямого цианирования. Золото в упорных сульфидных рудах вкраплено в такие золотовмещающие минералы как арсенопирит и пирит. Для повышения извлечения золота цианированием разработан целый ряд технологий, которые позволяют разрушать кристаллическую решетку золотовмещающих сульфидных минералов: обжиг, атмосферное выщелачивание, автоклавное окисление, а также биоокисление. Биоокисление арсенопирита и пирита может происходить в соответствии с суммарными уравнениями:
- 2FeAsS + 7O2 +H2SO4 + 2H2O→2H3AsO4 + Fe2(SO4)3
- 4FeS2 + 15O2 + 2H2O→2Fe2(SO4)3 + 2H2SO4
Деструкция сульфидных золотовмещающих минералов позволяет увеличить степень извлечения золота цианированием. Таким образом, биоокисление (как и обжиг, а также другие процессы окислительного выщелачивания) применяются для предобработки упорных сульфидных золотосодержащих руд и концентратов для дальнейшего цианирования, а само золото непосредственно при биоокислении сульфидных минералов практически не подвергается трансформации.
Процессы биовыщелачивания также применяются для извлечения урана из руд. Уран не содержится непосредственно в сульфидных минералах, однако окисленные минералы урана U(IV), например уранинит (UO2) могут подвергаться окислительному выщелачиванию ионами Fe3+, которые протекают со значительно большей скоростью, чем сернокислотное выщелачивание:
- UO2 + Fe2(SO4)3 → UO2SO4 + 2FeSO4
Так как при биоокислении сульфидных минералов, которые также содержатся в урановых рудах, происходит генерация ионов Fe3+, то окислительная активность микроорганизмов косвенно способствуют повышению скорости выщелачивания урана.
Технологически биогидрометаллургические технологии могут реализовываться различным образом как процессы отвального, кучного, подземного и чанового (реакторного или агитационного) биоокисление. Отвальное, кучное и поздземное биовыщелачивание осуществляются аналогично процессам химического выщелачивания (кислотного выщелачивания, цианирование и т.д.), но процессы биовыщелачивания предполагают циркуляцию раствора, содержащего кислоту, окислитель (Fe3+), генерируемый микроорганизмами, а также клетки микроорганизмов, а также принудительную аэрацию раствора и рудного штабеля для поддержания активности микроорганизмов. Чановое или реакторное биовыщелачивание подразумевает проведение окисления измельченного сырья (обычно концентратов) в реакторах с механическим перемешиванием. Процессы проводят в цепи реакторов (объемом от нескольких десятков до 1000 м3), соединенных последовательно и снабженных системами для поддержания стабильных физико-химических параметров пульпы (температуры, pH), а также аэрации. Благодаря обеспечению интенсивного перемешивания и аэрации чановое биовыщелачивание обеспечивает переработку сырья с большей скоростью, но требует гораздо больших капитальных и эксплуатационных затрат по сравнению с процессами кучного, отвального и подземного биовыщелачивания.
Так как особенности разных биогидрометаллургических технологий обуславливают различия в капитальных и эксплуатационных затратах, то они также определяют и выбор технологической схемы для переработки различных типов сырья. Например, процессы кучного выщелачивания благодаря низким затратам успешно используется для переработки бедных руд цветных металлов, прежде всего меди. В переработку вовлекаются руды с содержанием меди от 0.15 до 2%. Масса эксплуатируемых куч бедных медных руд может достигать нескольких миллионов тонн, время их эксплуатации – нескольких лет. По разным оценкам от 5 до 15% мирового производства меди обеспечивается кучным биовыщелачиванием, которое применяется в разных странах и регионах (КНР, Южная и Северная Америка). Меньший вклад процессы кучного, отвального и подземного биовыщелачивания вносят также в добычу других металлов (никель, цинк, уран). Реакторное биоокисление обычно применяется для переработки сульфидных концентратов золотосодержащих руд, чтобы сделать рентабельной данную технологию, требующую относительно высоких затрат. В настоящее время в мире насчитывается около полутора десятков предприятий, использующих реакторное биоокисление для получения золота, в том числе крупные ГОКи, такие как Олимпиаднинский ГОК в Красноярском крае (Россия). Вклад процессов реакторного биовыщелачивания в общемировую добычу золота оценивается примерно в 5%.
Процессы биовыщелачивания обладают целым рядом преимуществ, которые обуславливают их распространенность по всему миру. Процессы биовыщелачивания позволяют извлекать цветные металлы из сульфидных и смешанных руд с большей скоростью, чем кислотное выщелачивание, а также снизить потребление серной кислоты благодаря ее биологической генерации в процессе окисления соединений серы. Основными преимуществами процессов биовыщелачивания являются относительно низкие капитальные затраты из-за отсутствия сложного оборудования, а также относительно низкое воздействие на окружающую среду (прежде всего из-за отсутствия газовых выбросов, что важно, прежде всего, для переработки сырья, содержащего мышьяк) и невысокое энергопотребление. Эффективность процессов биовыщелачивания зависит в большой степени от активности микроорганизмов, осуществляющих биоокисления, а также от целого ряда других факторов.
К факторам, которые определяют активность микроорганизмов в промышленных процессах биовыщелачивания, являются интенсивность аэрации, доступность углерода (который в основном поступает вместе с воздухом при аэрации в виде диоксида углерода) и других элементов (азот, фосфор) для конструктивного метаболизма микроорганизмов, а также физико-химические параметры такие как pH, температура и концентрация токсичных ионов в среде (тяжелые металлы, мышьяк). Необходимо отметить, что такие параметры как pH среды и температура изменяются из-за биоокисления сульфидных минералов, которые входят в состав руд и концентратов и должны регулироваться при проведении технологических процессов. Например, pH рекомендуется поддерживать в диапазоне 1.2−2.0, так как значения pH выше и ниже данного диапазона может приводить как к подавлению активности микроорганизмов, так и к образованию вторичных осадков (гидроксосульфатов железа Fe3+), что также снижает эффективность выщелачивания. Так как процессы окисления сульфидных минералов сопровождаются выделением тепла, в технологических процессах может происходить нежелательное повышение температуры, что требует использования систем охлаждения при проведении реакторного биовыщелачивания. Кроме того, эффективность биовыщелачивания определяется целым рядом технологических параметров, включая крупность руд и концентратов, продолжительность процессов, интенсивность перемешивания и газообмена, плотность пульпы, а также минеральным составом окисляемых руд и концентратов и соотношения разных сульфидных минералов в перерабатываемом сырье. Все эти факторы должны учитываться при осуществлении процессов биовыщелачивания, а в ходе испытаний для конкретного образца минерального сырья должны определяться оптимальные параметры для его переработки.
Таким образом, процессы биовыщелачивания сульфидных минералов служат основой для используемых на практике технологий, применяемых для переработки некоторых типов минерального сырья и продуктов обогащения (сульфидные руды и концентраты), которые успешно конкурируют с альтернативными технологиями благодаря ряду преимуществ. Для успешного внедрения биогидрометаллургических процессов должен учитываться целый ряд факторов, позволяющих оптимизировать технологические процессы и поддерживать активность биологических процессов на требуемом уровне.
Исследовательской группой было изучено как распространение ацидофильных микроорганизмов на изучаемых месторождениях, так и возможность извлечения урана из образца руды с применением полученных культур ацидофильных микроорганизмов.
Члены исследовательской групп также уже на протяжении почти пяти лет работают в направлении изучения гидрохимических методов переработки и методов биовыщелачивания урансодержащих руд и промышленных отходов.
Различные ацидофильные микроорганизмы широко распространены на месторождениях сульфидных руд, в том числе урановых. Отвалы пустой породы и отработанные штабели кучного выщелачивания урановых руд являются благоприятными местами обитания для ацидофильных микроорганизмов, так как в процессе добычи руды, укладки штабелей руды для последующего выщелачивания и отвалов пустой породы создаются условия для контакта сульфидных минералов руды с атмосферным воздухом, а также водой (выщелачивающими растворами, атмосферными осадками). Описанные процессы приводят к активному росту аборигенных микроорганизмов, который в естественных условиях может быть ограничен в силу отсутствия доступа кислорода в местах залегания сульфидных минералов. Процессы развития ацидофильной микробиоты на объектах кучного выщелачивания могут играть двоякую роль. С одной стороны, ацидофильные микроорганизмы применяются в процессах кучного выщелачивания различных руд, содержащих сульфидные минералы (в т.ч. урановых). При этом самопроизвольное развитие микробиоты в процессах кислотного выщелачивания сульфидных руд может приводить к интенсификации процесса выщелачивания, так как процессы биоокисления приводят к генерации серной кислоты и ионов Fe3+, что, в свою очередь, увеличивает скорость окисления сульфидных минералов руды и выщелачивания целевых компонентов. При этом развитие ацидофильной микробиоты может также приводить к нежелательным экологическим последствиям, что часто происходит в местах складирования отходов добычи, обогащения и переработки сульфидных руд, так как на подобных объектах в силу контакта отходов, содержащих сульфидные минералы, с атмосферным воздухом, также происходит активное развитие ацидофильных микроорганизмов, что приводит к протеканию биогеохимических процессов, аналогичных тем, которые применяются для биовыщелачивания руд. При протекании самопроизвольных процессов биовыщелачивания в отвалах отходов добычи, обогащения и переработки руд неизбежны негативные последствия для окружающей среды в силу неконтролируемого образования и распространения кислых сточных вод, содержащих ионы тяжелых металлов. Следствием таких процессов является миграция ионов тяжелых металлов, в т.ч. их попадание в грунтовые воды и водоемы. Поэтому изучение ацидофильной микробиоты с целью понимания ее видового состава, закономерностей ее развития и возможности регуляции ее активности в технологических процессах, а также при хранении отходов является важной исследовательской задачей. При этом места обитания, благоприятные для развития ацидофильных микроорганизмов, которые участвуют в окислении сульфидных минералов, являются источников для выделения биотехнологически значимых штаммов микроорганизмов. Исследования ацидофильных микробных популяций может проводится целым рядом методов, включая классические микробиологические (культуральные), которые позволяют получить накопительные и чистые культуры микроорганизмов, пригодные для применения в биотехнологических процессах, с помощью посевов на питательные среды, содержащие сульфат железа (II) и/или соединения серы, так и с помощью молекулярно-биологических, которые позволяют как определить состав микробных популяций без выделения чистых культур микроорганизмов, так и провести идентификацию выделенных чистых культур микроорганизмов. Используемые в данных целях молекулярно-биологические методы основаны на секвенировании генов 16S рРНК, который является универсальным маркерным геном для идентификации микроорганизмов. При этом для определения состава микробных популяций применяется выскопроивзодительное секвенирование (или NGS секвенирование) и секвенирование гипервариабельных участков гена. Такие подходы позволяют выявить присутствие в микробных популяциях микроорганизмов различных таксономических групп, а также отслеживать изменения относительной численности разных групп микроорганизмов в технологических процессах. Идентификация чистых культур микроорганизмов требует секвенирования полной последовательности гена 16S рРНК. Таким образом, применяемые современные методы позволяют как установить состав микробных популяций в разных местах обитания, так и получить культуры микроорганизмов для использования в технологических процессах.
Исследования на участках кучного выщелачивания рудника Шантобе позволили получить культуры железоокисляющих бактерий с применением питательной среды 9К. С использованием секвенирования гена 16S rRNA было определено таксономическое положение идентифиицруемых штаммов: царство - Bacteria, тип - Proteobacteria, класс - Acidithiobacillia, порядок - Acidithiobacillales, семейство - Acidithiobacillaceae, род - Acidithiobacillus, вид - Acidithiobacillus ferrooxidans. Бактерии вида Acidthiobacillus ferrooxidans характеризуются способностью в кислых растворах окислять железо (II) в присутствии серной кислоты, а также восстановленные соединения серы, а также устойчивостью к низким значениям pH и высоким концентрациям ионов металлов. Это определяет возможность использования данных бактерий в процессах кучного выщелачивания урансодержащих руд. Поэтому выделенные штаммы бактерий были использованы для проведения лабораторных испытаний по выщелачиванию урансодержащей руды.
Необходимо отметить, что в процессы обогащения в качестве сырья вовлекаются бедные и забалансовые руды, а также отходы горнообогатительного производства, что позволяет увеличиват сырьевую базу и значительно увеличат производство металлов. Проведенные испытания по выщелачиванию пробы урансодержащей руды показали высокую эффективность выщелачивания руды с помощью бактериально-химического способа. Сравнительный анализ испытаний на руде различной крупности, а также проведение контрольных испытаний без добавления бактерий показал, что бактериально –химическое выщелачивание для данного типа руды в 2-3 раза кинетически эффективной чем без использования бактерий.
Для проведения эксперимента использовали отобранную пробу руды крупностью – 0,055 мм, содержащую 0,285% U в виде уранинита. Плотность пульпы в экспериментах составила 25% (Т:Ж=1:4). Выщелачивание проводили на шейкере при 180 об/мин при температуре 28°С. Время выщелачивания составило от 4 до 16 часов.
Исследовали влияния концентрации выщелачивающего реагента (серной кислоты) на извлечение урана. Для этого проводили выщелачивание пробы руды растворами H2SO4 с концентрацией от 10 до 30 г/л. Результаты экспериментов по выщелачиванию показаны в таблице 16.
Таблица 1. Результаты выщелачивания урана с помощью растворов серной кислоты
| Концентрация H2SO4, г/л | 10 | 15 | 20 | 25 | 30 |
| Извлечение урана, % | 1,5 | 1,9 | 9,9 | 17,9 | 19,4 |
Даже при выщелачивании раствором с самой высокой концентрацией H2SO4 (до 30 г/л) степень выщелачивания урана была невысокой (19.4%). Расход серной кислоты был высоким и составил от 50 до 150 кг/т.
Таким образом, было показано, что выщелачивание с помощью растворов серной кислоты без внесения окислителей не позволило достигнуть высокой степени извлечения урана, что соответствует результатам теоретического анализа известных технологий выщелачивания урана. Поэтому далее исследовали процесс выщелачивания урана с использованием различных реагентов-окислителей: сульфат железа (III) Fe2(SO4)3, надсернокислый аммоний (NH4)2S2O8 и перманганат калия KMnO4 в растворах с различной концентрацией. В экспериментах с данными окислителями концентрация H2SO4 в растворе составляла 20 г/л.
Результаты экспериментов представлены на рисунках 27-29. Все использованные окислители позволили поднять степень извлечения урана по сравнению с кислотным выщелачиванием. В экспериментах с сульфатом трехвалентного железа (1,16–5,8 г/л) повышение концентрации ионов трехвалентного железа приводило к повышению степени извлечения урана. Максимальная степень извлечения урана в раствор была максимальной (68%) при концентрации сульфата трехвалентного железа 5,8 г/л.
В экспериментах с персульфатом аммония в качестве окислителя его концентрация составила от 2,5 до 30 г/л. Было показано, что степень извлечения урана в раствор была максимальной (95,2%) в присутствии максимальной концентрации окислителя. Результаты экспериментов по выщелачиванию урана перманганатом калия (в концентрации от 0,5 до 3 г/л) представлены на рисунке 29. Было установлено, что в присутствии 1,5-3,0 г/л перманганата калия степень выщелачивания урана составила от 64,0 до 69,6%. Таким образом, персульфат аммония был наиболее эффективным для выщелачивания урана из руды.
Таким образом, степень выщелачивания U из бедной руды повышалась в присутствии изученных окислителей по сравнению с сернокислыми растворами и зависела от их концентрации. Наиболее высокие степени выщелачивания урана были достигнуты в экспериментах с персульфатом аммония.
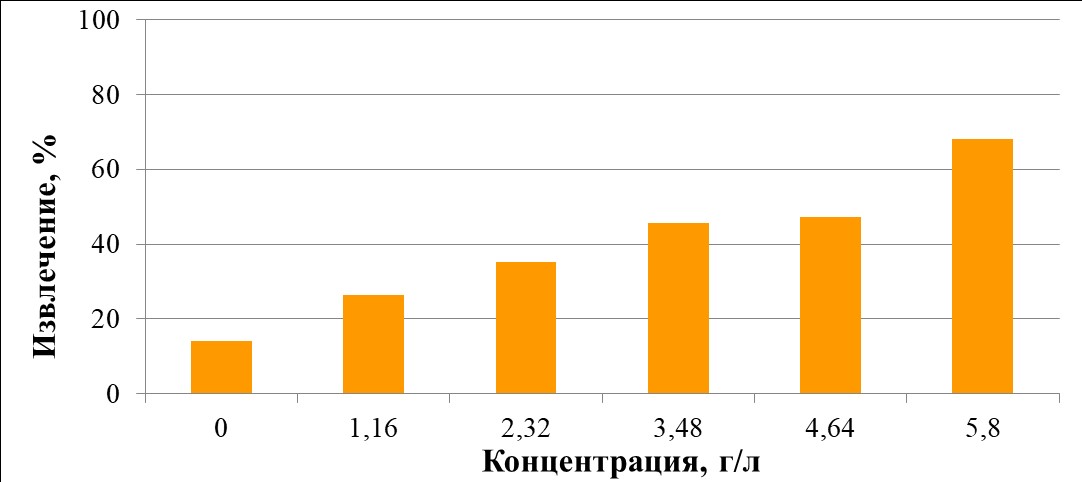
Выщелачивание урана растворами Fe2(SO4)3
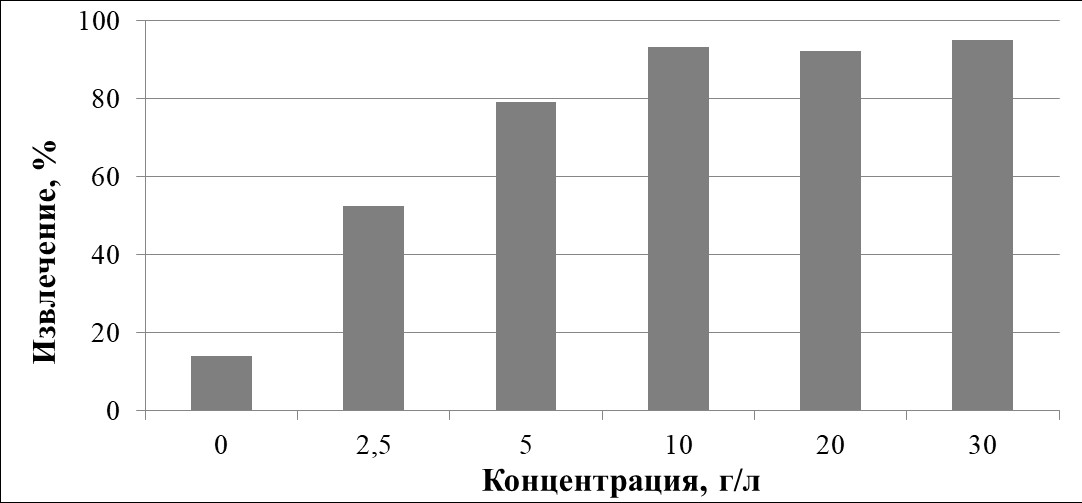
Выщелачивание урана растворами (NH4)2S2O8
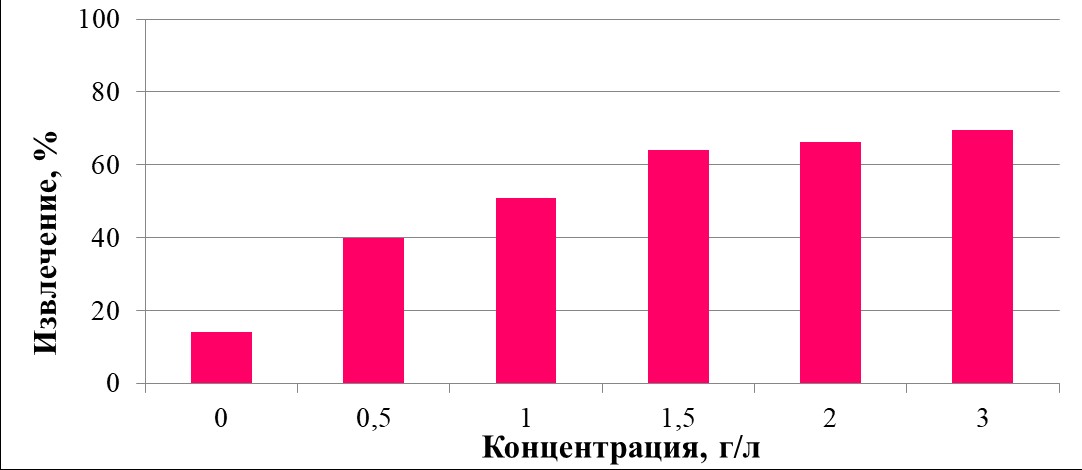
Выщелачивание урана растворами KMnO4
Для определения влияния на процесс выщелачивания урана времени выщелачивания и присутствия в среде клеток микроорганизмов, провели эксперимент по выщелачиванию урана из руды с помощью пробы кислых подотвальных вод с pH около 1,5, которую использовали для выщелачивания, отобранная на месторождении «Восток», содержала 6,86 г/л Fe3+ и около 1 × 106 кл/мл бактерий A. ferrooxidans. Сопоставляли степень извлечения руды после 4, 8 и 16 ч выщелачивания. Результаты эксперимента показаны на рисунке 30.
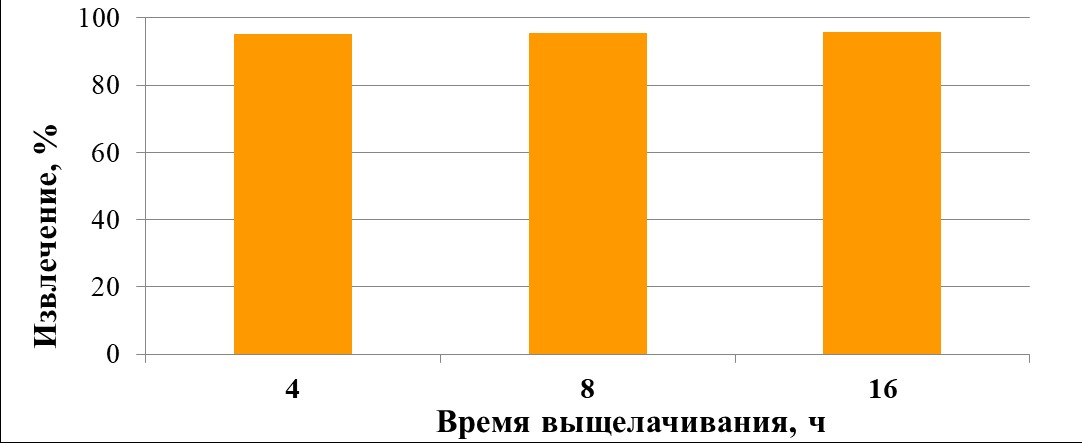
Выщелачивание кислой подотвальной водой
Было показано, что степень извлечения урана с помощью пробы подотвальной руды, которая содержала как окислитель (ионы Fe3+), так и клетки микроорганизмов, была значительно выше, чем с помощью раствора сульфата железа (III) (рисунки 27 и 30), что указывает на активацию процессов выщелачивания ацидофильными микроорганизмами.
Таким образом, было продемонстрировано, что может быть предложена принципиальная технологическая схема переработки урансодержащих руд с использованием бактерий A.ferrooxidans, так как применение биовыщелачивания позволяет добиться высокой степени извлечения урана без применения химических окислителей.

